基于SOPC的低電壓電泳芯片系統平臺設計
1 引 言
本文引用地址:http://www.j9360.com/article/192054.htm生物芯片的控制、檢測與分析是生物芯片技術中的重要組成部分,最早的應用起源于毛細管電泳芯片的檢測,其目的是實現基因片段的分離。從電泳芯片的研究現狀可以看出,目前研究主要是將毛細管電泳技術移植到以玻璃、硅、有機物等材料為基片的芯片中。利用電泳系統較短的分離溝道和良好的散熱特性,在較高的場強下完成快速、高效的分離分析。但由于其工作電壓高(一般在幾千伏左右)、體積較大、進樣、分離、檢測多為分離組裝式,實驗室局限性強,不適應在芯片上完成化學反應及檢測、分析的發展。為此近年來,設計開發低電壓、便攜式、高集成度的生物芯片控制與檢測系統一直以來是研究人員研究的熱點[1-4]。本文著重討論了基于Altera公司FPGA的嵌入式處理器NiosII內核及SOPC軟、硬件設計技術在低電壓毛細管電泳芯片 (Low Voltage Integrated Capillary Electrophoresis Chip, LVICEC)控制與采集系統中的應用。
2 LVICEC運動梯度電勢控制原理
毛細管電泳芯片通常以玻璃、石英、硅、塑料等為基質,運用MEMS加工技術刻蝕出直徑為微米級的通道網絡,在這些網絡中,以電場為驅動力,根據不同離子、分子、以及細胞在電場作用下運動速度的不同,對混合物(離子、分子、細胞等)實現分離。通常采用的電泳電壓為高電壓,如Jacobson等所采用的 35KV/cm。較高的分離電壓制約了電泳芯片向集成化、便攜式、低成本的方向發展[5]。而低電壓分離的思想在于,在電泳分離的通道上,按一定控制算法,分段、運動式交替施加分離電壓,在較短長度的分離通道上采用低電壓供電方式得到較高電場分布,其控制原理及運動模型見圖1所示。
設分離電壓為V,初始分離間距為2a, 分別為第j 次所加的場強、循環次數、電壓施加的時間及第j次分離完成后的總分離長度。分離過程中,首先在分離電極陣列1,3之間施加電壓V(E1=V/2a),驅動樣品組分向正方向運動,在恒定的時間t1段內,以恒定的電場強度E1將電壓V施加在2,4分離電極陣列之間,依次類推,直至以t1和E1為控制時間和分離場強的第1階段的循環次數c1結束,然后增加電壓所施加的長度E2=V/3a進入控制時間為t2分離場強為E2循環次數為c2的第2階段,如此遞推,在分離通道上分段、交替循環地施加分離電壓,從而形成運動的梯度電勢完成樣品組分的分離。
圖1 低電壓毛細管電泳芯片控制原理及運動模型示意圖
3 低電壓電泳芯片系統硬件平臺的設計
3.1 系統硬件的設計方案
系統的設計思想是先通過負壓進樣后,在低電壓運動控制器的作用下,分段、交替輸出分離電壓到分離電極上,形成一定的運動梯度電場,待分離組分在梯度電場的作用下,呈現出不同的分離速率,后經檢測器處的信號采集電路,在NIOSII處理器的控制下將電泳信號保存到存儲器中,通過一定的信息輸出方式,最終將電泳信號傳到PC機中,進行后續的電泳圖譜分析與處理。基于SOPC的低電壓電泳芯片控制與采集硬件系統主要由低電壓電泳芯片、負壓進樣控制電路、低電壓運動電壓控制模塊、電泳信號采集及處理電路模塊、SDRAM存儲器、閃速存儲器flash、操作控制輸入電路、信息輸出電路等部分組成。
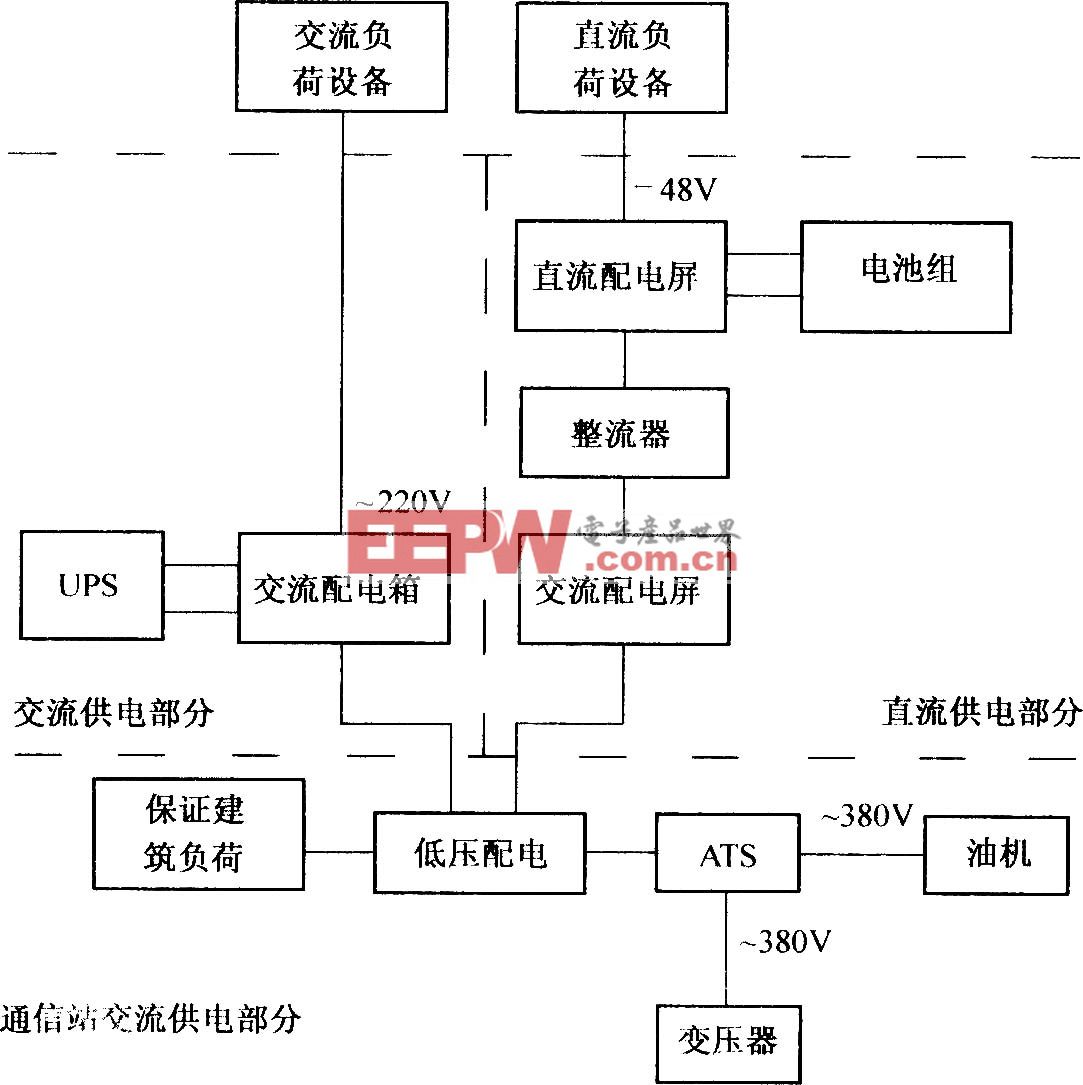
基于SOPC 的低電壓電泳芯片系統平臺硬件的總體設計方案如圖2所示。
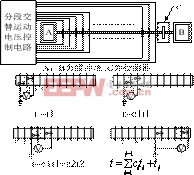
圖2 系統總體設計框圖
低電壓毛細管電泳芯片采用MEMS加工技術,在ITO玻璃基片上經清洗、烘干、正膠光刻ITO圖形、濕法腐蝕ITO薄膜、去膠、清洗、烘干等工藝后形成低電壓微電極陣列及電導檢測器,在玻璃蓋片上經清洗、烘干、負膠光刻、濕法腐蝕、去膠、清洗、烘干等工藝后形成緩沖池、進樣溝道以及分離溝道,最后經玻-玻鍵合制備而成。




評論