FDA批準首個用于心衰的植入式遠程無線監測設備

2014年5月28日,美國食品和藥品管理局(FDA)批準了第一個用于心衰患者的無線、植入式血流動力學監測系統——CardioMEMS,認為該系統的效果和安全性具有合理保證,能夠用于目標心衰患者的管理并減少心衰相關的住院率。
CardioMEMS(Champion HF Monitoring System ,Champion心衰監測系統)可測量患者的平均肺動脈壓和心率,被批準用于過去1年內有心衰住院史的NYHA 3級患者。
FDA批準該系統主要是基于CHAMPION研究,這是一項開放標簽研究。研究結果顯示,在伴有呼吸困難的NYHA 3級心衰患者中,植入肺動脈壓力傳感器組與標準治療組相比住院減少30%。
2013年,FDA顧問小組以6:4微弱投票優勢贊成批準該永久植入的診斷裝置,認為它有較好的風險獲益比。但在2011年,FDA顧問小組曾投票反對批準該裝置。
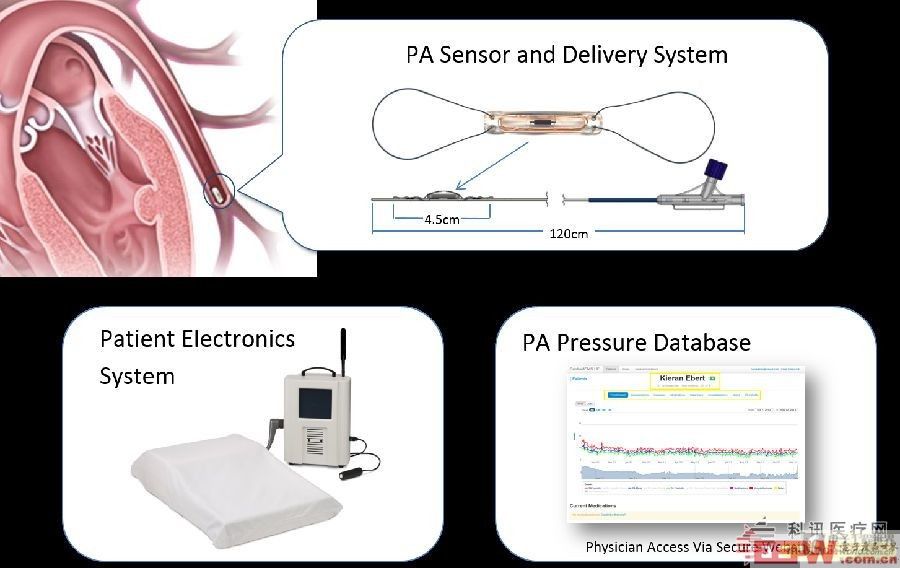
附:CardioMEMS裝置介紹
該裝置由一個經靜脈導管置入的傳感器和一個電子系統,后者從傳感器獲取并處理信號,然后將肺動脈壓信息傳遞到安全數據庫。遵照程序,病人在家里無線監測其肺動脈壓力,數據立即傳送到安全的數據庫,供醫生可通過CardioMEMS網站實時監測。









評論